| БЕЛКИ ОСТРОЙ ФАЗЫ ВОСПАЛЕНИЯ |
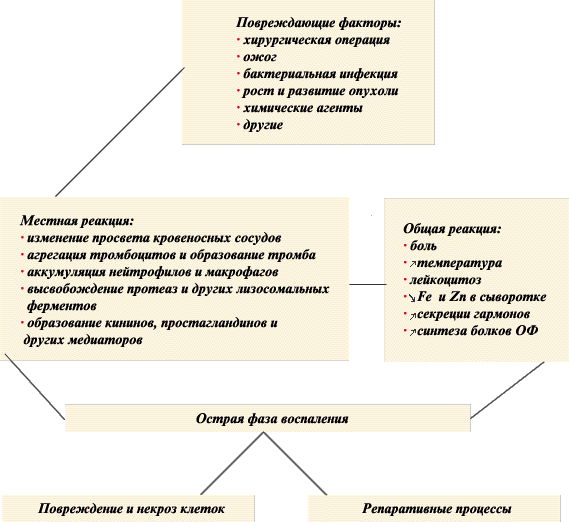
В ответ на любое повреждение, будь то физическая травма, ожог, хирургическая операция, инфекция и др., в организме развивается целый комплекс физиологических реакций, направленных на локализацию очага повреждения и скорейшее восстановление нарушенных функций. Этот сложный процесс, направленный на сохранение гомеостаза, известен как воспаление, а комплекс местных и системных изменений, возникающих непосредственно вслед за повреждением, в совокупности составляет понятие острой фазы воспаления.

Рис. 1. Схема реакции острой фазы воспаления
Издревле известны классические признаки воспаления: tumor, rubor, color, dolor. Более полное представление о развитии этого феномена и месте белков острой фазы дает схема (рис. 1). У человека, как и у других млекопитающих, острая фаза воспалительного ответа характеризуется повышением температуры, изменением проницаемости сосудов, изменением биосинтетического и метаболического профиля многих органов. В развитии ОФ участвуют системы всего организма: иммунная, центральная нервная, эндокринная, сердечно-сосудистая. Важнейший аспект ОФ - радикальное изменение биосинтеза белков в печени. Понятие "белки острой фазы" объединяет до 30 белков плазмы крови, так или иначе участвующих в совокупности реакции воспалительного ответа организма на повреждение. Белки ОФ синтезируются в печени, их концентрация существенно изменяется и зависит от стадии, течения заболевания и массивности повреждения, что и определяет ценность этих тестов для клинической лабораторной диагностики.
| Для острой фазы
воспаления характерны: —» неспецифичность и универсальность; сходный комплекс реакций мотнет развиться как при инфекции, так и после физической травмы; —»
направленность на ограничение
очага повреждения,
осуществление репаративных
процессов. |
| РЕГУЛЯЦИЯ И КОНТРОЛЬ СИНТЕЗА БЕЛКОВ ОФ |
Развитие острой фазы воспалительного ответа инициируется и регулируется целым рядом медиаторов, среди которых цитокины, анафилотоксины и глюкокортикоиды. Некоторые из них выделяются непосредственно в очаге воспаления активированными макрофагами, лимфоцитами и другими клетками и могут оказывать как местное, так и общее воздействие. Наиболее важные растворимые факторы, регулирующие синтез белков ОФ в печени, показаны на рис. 2. Условно их можно разделить на 4 группы:
1. ИЛ-6 и сходные с ним по действию (ИЛ-1 1, онкостатин М и др.).
2. ИЛ-1 и сходные с ним по действию ( ИЛ-1 а, ИЛ-1Р, факторы некроза опухолей ФНО-ОС и ФНО-Р).
3. Глюкокортикоиды.
4. Факторы роста, к числу которых относятся инсулин, факторы роста гепатоцитов, фибробластов, тромбоцитов. Регуляция синтеза белков ОФ не является универсальной. Это сложный многофакторный механизм, отдельный для каждого белка. Каждый из цитокинов выполняет уникальную, независимую функцию. В общих чертах можно представить, что цитокины действуют как первичные стимуляторы генной экспрессии, глюкокортикоиды и факторы роста являются модуляторами действия цитокинов.
Как правило, концентрация белков ОФ увеличивается в течение первых 24-48 часов. Классически ОФ длится несколько дней, что указывает на защитную, гомеостатическую природу этого важного ответа. Однако нормальный цикл может быть пролонгирован при продолжении действия повреждающих факторов или при нарушении механизмов контроля и регуляции. Окончательно неизвестно, какое контрольное звено является критическим для конверсии острофазного ответа в хроническую фазу воспаления. Но безусловно ясно, что при нарушении механизмов регуляции ОФ повреждение тканей может продолжаться и привести к развитию последующих осложнений, например, сердечно-сосудистых заболеваний, болезней накопления, таких как реактивный амилоидоз.
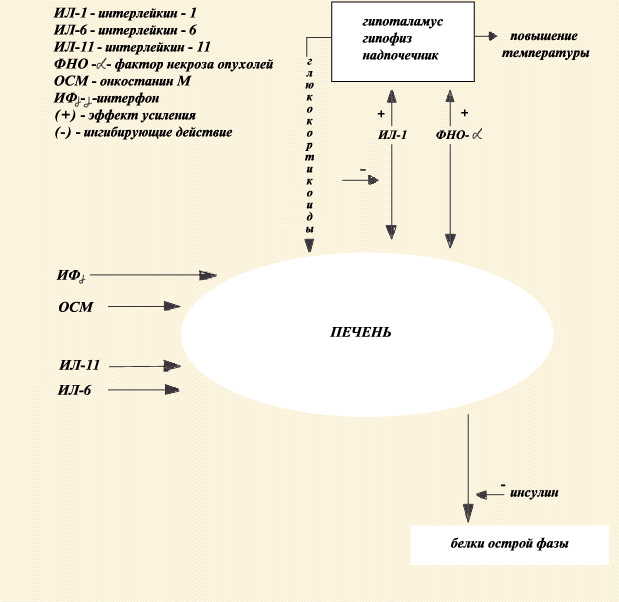
Рис. 2. Схема регуляции синтеза белков ОФ в печени.
| ОФ длится 7-10
дней, что указывает на защитную
и гомеостатическую природу этого важного
ответа. Точно не известно, какое звено является критическим для конверсии в хроническую фазу воспалительного процесса. |
| ХАРАКТЕРИСТИКА И КЛАССИФИКАЦИЯ БЕЛКОВ ОФ |
Особенностью большинства белков ОФ является их неспецифичность и высокая корреляция концентраций в крови с активностью заболевания, стадией процесса. Это выгодно отличает белки ОФ от других широко используемых маркеров воспаления, таких как скорость оседания эритроцитов (СОЭ), подсчет количества лейкоцитов и сдвиг лейкоцитарной формулы. В связи с этим ценность тестов на белки ОФ для мониторинга течения заболеваний и контроля эффективности лечения трудно переоценить. В то же время диагностическая значимость этих тестов, в силу их неспецифичности, может быть весьма ограниченной.
Изменение концентрации различных белков в условиях повреждения и воспаления варьирует в широких пределах. Далее представлена классификация белков ОФ в зависимости от степени увеличения их концентрации при физической травме.
1. К «главным» белкам ОФ у человека относят С-реактивный белок (СРВ) и амилоидный А белок сыворотки крови (см. таблицу, 1). Уровень этих белков возрастает при повреждении очень быстро (в первые 6-8 часов) и значительно (в 20-100 раз, в отдельных случаях - в 1000 раз).
Классификация белков ОФ но степени увеличения их концентрации
1. |
«Главные» реактанты ОФ, увеличение концентрации в 100-1000 раз в течение 6-12 ч |
| Белок | Концентрация в сыворотке крови здорового человека (г/л) |
| С-реактивный белок (СРБ) Амилоидный белок А сыворотки |
< 0.005 |
2. Вторую группу составляют белки, концентрация которых может увеличиваться существенно (в 2-5 раз) (см. таблицу, 2). Тесты на кислый a1-гликопротеид (орозомукоид), a1-антитрипсин (a1-ингибитор протеиназ), фибриноген, гаптоглобин имеют очевидную информативность при многих заболеваниях.
(Продолжение)
2. |
Умеренное увеличение концентрации (в 2-5 раз) в течение 24 ч |
| Белок | Концентрация в сыворотке крови здорового человека (г/л) |
| Орозомукоид (кислый a1-гликопротеид) | 0,4 - 1,3 |
| a1- Антитрипсин | 1,4 - 3,2 |
| Гаптоглобин | 0,5 - 3,2 |
| Фибриноген | 1,8 - 3,5 (плазма) |
3. Индивидуальной оценки требует интерпретация результатов , измерения концентраций церулоплазмина, С3-компонента комплемента, уровень которых увеличивается на 20-60% от исходного (см. таблицу 3), и в ряде случаев может не превышать пределов диапазона вариаций нормальных концентраций этих белков в плазме крови здорового человека.
(Продолжение)
3. |
Незначительное увеличение концентрации (на 20 - 60%) в течение 48 ч |
| Белок | Концентрация в сыворотке крови здорового человека (г/л) |
| Церулоплазмин | 0,2 - 0,5 |
| C3 - комплект | 0,5 - 0,9 |
| C4 - комплект | 0,1 - 0,4 |
4. К так называемым нейтральным реактантам ОФ относят белки, концентрация которых может оставаться в пределах нормальных значений, однако они принимают участие в реакциях острой фазы воспаления. Это a1 - макроглобулин, гемопексин, амилоидный Р белок сыворотки крови, иммуноглобулины (см. таблицу, 4).
(Продолжение)
4. |
Нейтральные реактанты ОФ |
| Белок | Концентрация в сыворотке крови здорового человека (г/л) |
| Иммуноглобулин G | 8 - 20 |
| Иммуноглобулин A | 0,9 - 4,5 |
| Иммуноглобулин M | 0,6 - 2,5 |
| a2 - Макроглобулин | 1,2 - 3,2 |
5. Содержание «негативных» реактантов ОФ может снижаться на 30-60%. Наиболее диагностически значимые из этой группы белков - альбумин, трансферрин, a-липопротеид, преальбумин (см. таблицу, 5). Уменьшение концентрации отдельных белков в острой фазе воспаления может быть обусловлено снижением синтеза, увеличением потребления, либо изменением их распределения в организме.
(Продолжение)
5. |
"Негативные" реактанты ОФ, уровень может снижаться в течение 12 - 18 ч |
| Белок | Концентрация в сыворотке крови здорового человека (г/л) |
| Альбумин | 37 - 53 |
| Трансферрин | 2,3 - 4,3 |
| Преальбумин | 0,25 - 0,45 |
Как видно из таблицы, к острофазным относят белки с различной биологической функцией. Все они выполняют важную роль в месте повреждения или на уровне организма и непосредственно участвуют в осуществлении комплекса реакций, направленных на удаление повреждающего фактора, локализацию очага повреждения, восстановление нарушенной структуры и функции.
Так, С-реактивный белок способен связывать широкий спектр лигандов-компонентов микроорганизмов, токсинов, частиц поврежденных тканей, препятствуя тем самым их распространению. Кроме того, продукты такого взаимодействия активируют комплемент по классическому пути, стимулируя процессы фагоцитоза и элиминации вредных продуктов. С-реактивный белок может взаимодействовать с Т-лимфоцитами, фагоцитами и тромбоцитами, регулируя их функции в условиях воспаления. Орозомукоид (кислый a1 - гликопротеид) обладает антигепариновой активностью, при повышении концентрации этого белка в сыворотке ингибируется агрегация тромбоцитов.
Фибриноген не только является важнейшим из белков свертывания крови, но также и источником образования фибринопептидов, обладающих противовоспалительной активностью.
Церулоплазмин является поливалентным окислителем (оксидазой), он инактивирует супероксидные анионные радикалы, образующиеся при воспалении, защищая тем самым биологические мембраны.
Гаптоглобин не только способен связывать гемоглобин с образованием комплекса, обладающего пероксидазной активностью, но достаточно эффективно ингибирует катепсины С, В и L. Гаптоглобин может участвовать в утилизации некоторых патогенных бактерий и в будущем предполагается его использование для лечения некоторых инфекций.
Целый ряд белков острой фазы обладает антипротеазной активностью. Это a1-ингибитор протеиназ (a1-антитрипсин), антихимотрипсин, a2- макроглобулин. Их важная функция состоит в ингибировании активности эластазоподобных и химотрипсиноподобных протеиназ, поступающих из гранулоцитов в воспалительные экссудаты и вызывающих вторичное повреждение тканей. Для начальных стадий острого воспаления обычно характерно снижение уровней ингибиторов, вслед за этим происходит повышение концентрации, связанное с увеличением синтеза этих белков. Снижение уровней ингибиторов протеиназ при септическом шоке или остром панкреатите является плохим прогностическим признаком. Специфические ингибиторы протеолитических каскадных систем, комплемента, коагуляции и фибринолиза регулируют изменение активности этих важнейших биохимических путей в условиях воспаления.
| Белки ОФ - широкий
спектр белков плазмы крови,
обладающих различной
функциональной активностью и
играющих важную роль в
защитных реакциях организма
при воспалении. Степень и скорость изменения концентрации различных белков ОФ существенно различаются. Правильный выбор и адекватная интерпретация результатов тестов на белки ОФ необходимы для их успешного применения в клинической практике. |
| КАК ОПРЕДЕЛЯТЬ БЕЛКИ ОФ |
Общие требования к методам, используемым для тестирования белков острой фазы, нетрудно сформулировать, учитывая приведенные выше сведения.
Это, в первую очередь, необходимость количественного анализа концентрации белка. Диагностическая значимость белков ОФ состоит именно в возможности уловить изменение их концентраций в зависимости от стадии заболевания, эффективности (или, напротив, неэффективности) лечения, массивности поражения, что возможно только при условии количественного измерения,
Также очевидно, если требуется измерение динамики концентраций белков в процессе заболевания, то метод должен тиражироваться и хорошо воспроизводиться, чтобы позволять получать сравниваемые результаты.
Безусловно, по этой же причине тесты на белки ОФ должны быть доступны и экономичны в отношении их трудоемкости и стоимости.
Чувствительность метода должна быть адекватной для исследования белков ОФ. Из таблицы видно, что диапазон диагностически значимых концентраций большинства белков ОФ измеряется десятками-сотнями мг/л. Поэтому для их определения должны использоваться не высокочувствительные, но высокоспецифичные количественные методы.
Основные методы, которые отвечают всем вышеперечисленным условиям и которые следует использовать для определения белков ОФ, следующие.
1.
Инструментальные: нефелометрия, иммунотурбидиметрия.
Эти два метода примерно
равноценны по
чувствительности,специфичности,
трудоемкости и стоимости
исследования. Поэтому выбор между
ними, как правило, определяется
обеспеченностью соответствующими
приборами и высокоспецифичными наборами
реагентов. Серийность и
автоматизация исследований делает
эти методы оптимальными для
больших и средних лабораторий,
выполняющих десятки и сотни
анализов в день.
2. Методы,
не требующие оборудования:
радиальная иммунодиффузия.
Полностью готовые к употреблению иммунодиффузионные планшеты
позволяют проводить
количественный анализ С-реактивного белка и других
белков ОФ без приборов и
дополнительных реагентов. Они
рекомендованы для небольших
лабораторий, выполняющих
ограниченное число исследований
(от одного до 20 анализов) в день.
Латекс-агглютинация может использоваться как быстрый полуколичественный метод определения С-реактивного белка, Его назначение - скрининг повышенных концентраций, после чего следует перейти к мониторингу с использованием количественных методов.
| Для
определения белков ОФ
необходимо использовать
количественные методы анализа
концентрации белка. Оптимальными инструментальными методами являются иммунотурбидиметрия и нефелометрия, позволяющие автоматизировать исследования и выполнять большое количество анализов ежедневно. Иммунодиффузионные планшеты (метод радиальной иммунодиффузии) позволяют определять белки ОФ без оборудования, а также могут быть рекомендованы для небольших лабораторий при ограниченном количестве исследований. Полуколичественный метод латекс-агглютинации предназначен для скринингового выявления повышенных концентраций С-реактивного белка. |
| КАКИЕ ТЕСТЫ НА БЕЛКИ ОФ СЛЕДУЕТ ИСПОЛЬЗОВАТЬ В КЛИНИЧЕСКОЙ ПРАКТИКЕ |
При острых воспалительных заболеваниях, сепсисе самым чувствительным и самым быстрым индикатором повреждения является С-реактивный белок. Для определения характера и наблюдения за течением хронических процессов, желательно следить за изменением концентрации сразу нескольких более медленно реагирующих маркеров ОФ - кислого С^-гликопротеида (орозомукоида), К]-ингибитора протеиназ. Использование только одного из маркеров воспаления рискованно, так как у разных больных возможен дисгармоничный острофазный ответ. Повышенное потребление гаптоглобина, СЗ-компонента комплемента, фибриногена может указывать на наличие другого патологического процесса, сопровождающего воспаление. Включение в исследование негативных белков ОФ, таких как альбумин, трансферрин, позволяет получить дополнительные данные о хроническом процессе, общем катаболизме белков, вовлеченности сосудов.
1. Белки ОФ при
остром заболевании. Во всех
случаях следует определять
С-реактивный белок, концентрация
которого повышается уже спустя 6-8
часов после его начала, при
отсутствии лечения достигая
максимума на 2-3 сутки. Наиболее
высокие уровни СРБ наблюдаются при
бактериальной инфекции (100
мг/л и
выше). При эффективной терапии
концентрация СРБ снижает-
ся уже на следующий день, если же
этого не происходит, с учетом
изменений уровней СРБ решается
вопрос о выборе необходимого
антибактериального лечения.
При подозрении на сепсис у новорожденных концентрация СРБ более 12 мг/л является указанием на немедленное начало противомикробной терапии, но следует помнить, что у части новорожденных бактериальная инфекция может и не сопровождаться резким повышением концентрации СРБ.
При вирусной инфекции концентрация СРБ может повышаться лишь незначительно (меньше 20 мг/л), что используется для дифференцирования вирусной инфекции от бактериальной. Это имеет решающее значение у детей с менингитом: обнаружение СРБ в концентрации выше 20 мг/л является безусловным основанием для начала антибиотикотерапии.
При нейтропении у взрослого пациента обнаружение СРБ более 10 мг/л может оказаться единственным объективным указанием на наличие бактериальной инфекции и необходимость применения антибиотиков.
Если в последующие 4-5 дней после хирургической операции концентрация СРБ продолжает оставаться высокой (или увеличивается), это указывает на развитие осложнений (пневмонии, тромбофлебита, раневого абсцесса).
| При острых
заболеваниях |
|||
|
|
||
2. Белки ОФ при сопутствующей бактериальной инфекции. При любых заболеваниях, либо после операции присоединение бактериальной инфекции, будь то местный процесс или сепсис, сопровождается повышением уровней белков ОФ.
| Сопутствующие инфекции | ||
| Присоединение
бактериальной инфекции СРБ>100 мг/л: |
|
|
3. Белки ОФ при некрозе тканей. Некроз тканей вызывает острофазный ответ, аналогичный таковому при бактериальной инфекции. Это возможно при инфаркте миокарда, опухолевом некрозе тканей почки, легкого, толстого кишечника. Если обнаруживается повышение концентрации белков ОФ, но не удается выявить явных признаков воспаления, следует обследовать больного на наличие злокачественного заболевания.
| Некроз тканей | ||
| Инфаркт
миокарда Опухоли |
|
|
4. Применение белков ОФ для контроля эффективности лечения хронических заболеваний.
Существует корреляция между активностью воспаления, массивностью повреждения тканей и концентрацией белков ОФ. При этом следует измерять в динамике концентрацию нескольких белков ОФ, что позволит быстро улавливать ответ на лечение.
Системные ревматические заболевания. Резко увеличиваются концентрации целого спектра белков ОФ при ревматоидном артрите, очень чувствительны эти тесты при уменьшении активности и эффективном лечении. При системном васкулите контроль за уровнями СРБ используется как объективный тест, позволяющий минимизировать дозы стероидов.
Воспалительные заболевания т^елудочно-кишечного тракта. Болезнь Крона сопровождается сильным острофазным ответом, при неспецифическом язвенном колите он незначителен. При функциональных расстройствах обычно концентрация белков ОФ не увеличена.
При злокачественных опухолях возможны различные изменения концентраций белков ОФ, так как это зависит от присоединения инфекции, некроза тканей, нарушения функций органов вследствие возникновения непроходимости респираторных путей или желудочно-кишечного тракта, влияния иммуносупрессии и химиотерапии. Массивный острофазный ответ наблюдается при некрозе солидных опухолей. Лимфомы, напротив, редко сопровождаются тканевым некрозом и изменением спектра белков плазмы. При миеломе возможен очень сильный острофазный ответ, индуцированный повышенным синтезом ИЛ-6 опухолевыми клетками, что является плохим прогностическим признаком.
Вторичный амилоидоз. Повышение концентрации СРБ коррелирует с развитием почечных осложнений.
Отторжение трансплантата. При отторжении сердечного аллотрансплантанта концентрация СРБ не является хорошим тестом, но коррелирует с развитием инфекционных осложнений. А вот при отторжении почечного трансплантата острофазный ответ является одним из ранних индикаторов отторжения.
| Контроль эффективности лечения хронических заболеваний | ||
| Системные
ревматические заболевания
Болезни желудочно-кишечного тракта Отторжение трансплантата Вторичный амилоидоз и др. |
|
|
Литература
A. Koj: Metabolic studies of
acute-phase proteins.
Pathophysiology of plasma protein
metabolism, S221-248,
1984
H. Baumann & J. Gauldie: The acute phase response.
Immunologie Today, S74-80, No2, 1994