 (2)
(2)1. Предельно допустимые значения систематических и случайных погрешностей результатов клинических лабораторных исследований
В целях обеспечения единого уровня аналитической надежности клинических лабораторных исследований, соответствующего потребностям клинической диагностики и наблюдения за течением заболеваний пациентов и реально достижимого при имеющемся материально-техническом оснащении большинства клинико-диагностических лабораторий учреждений здравоохранения, вводятся рекомендуемые предельно допустимые значения (ПДЗ) смещения и общей вариации результатов клинических лабораторных исследований, предназначенные для использования при внутрилабораторном контроле качества (таблица
1). Рекомендуемые ПДЗ установлены путем экспертной оценки на основе сведений о биологической вариации компонентов биологических жидкостей и данных об аналитической вариации, полученных в рамках Федеральной системы внешней оценки качества клинических лабораторных исследований.
Рекомендуемые ПДЗ применяются при оценке допустимости погрешностей исследования контрольных материалов при внутрилабораторном контроле качества. ПДЗ смещения применяются для оценки допустимости систематической погрешности исследований и представляют собой предельно допустимые значения относительного смещения среднего арифметического результатов анализа в первых 10 (±B10, %) и 20 (±B20, %) аналитических сериях от установленных значений исследуемых показателей. ПДЗ общей вариации представляют собой значения коэффициентов вариации результатов, полученных в 10
(CV10, %) и 20 (CV20, %) аналитических сериях, и применяются для оценки допустимости случайных погрешностей.
В случае, если величины погрешностей в первых 10 и 20 аналитических сериях превышают установленные в
таблице 1 значения, заведующий лабораторией обязан принять меры по выявлению и устранению источников недопустимо больших погрешностей.
Устанавливаемые в соответствии с таблицей 1 ПДЗ вводятся как рекомендуемые и единые для всех клинико-диагностических лабораторий учреждений здравоохранения страны вне зависимости от ведомственной подчиненности и формы собственности. Соответствие получаемых в КДЛ результатов указанным нормам точности на данном этапе не должно использоваться в качестве критерия аккредитации клинико-диагностических лабораторий.
2. Биологически обоснованные нормы аналитической точности клинических лабораторных исследований и методика их расчета
Биологически обоснованные нормы аналитической точности клинических лабораторных исследований (таблица 2) представляют собой ПДЗ смещения и коэффициента общей аналитической вариации, рассчитанные исходя из коэффициентов внутри- и межиндивидуальной биологической вариации. Биологически обоснованные ПДЗ могут быть использованы в качестве перспективных (желательных) нормативов аналитической точности и могут вводиться по мере совершенствования оснащения лабораторий и повышения качества исследований в клинико-диагностической лаборатории по решению руководителя учреждения здравоохранения на основе рекомендации заведующего лабораторией.
Методика расчета биологически обоснованных норм аналитической точности
2.1. Принятые обозначения.
CVI - коэффициент внутрииндивидуальной биологической вариации, %
СVG - коэффициент межиндивидуальной биологической вариации, %
В - целевое значение смещения средней арифметической от установленного значения, %
СV - целевое значение коэффициента общей аналитической вариации, %
Bn - предельно допустимое значение смещения результатов, полученных в n аналитических сериях, %
CVn - предельно допустимое значение коэффициента вариации результатов, полученных в n аналитических сериях, %
n - число аналитических серий
2.2. Принципы расчета целевых значений.
Целевыми значениями требований точности анализа являются математические ожидания величин смещения среднего арифметического результатов от установленного значения (В) и коэффициента аналитической вариации (CV), которые могут быть достигнуты в клинико-диагностических лабораториях при бесконечно большом числе измерений. Расчет целевых значений производится исходя из величин внутрииндивидуальной (CVI) и межиндивидуальной биологической вариации (СVG) соответствующего показателя у здоровых людей. Источник сведений о биологической вариации - сводный банк данных, опубликованных M.A.Sebastian-Gambarо et al., 1997 .
M.A.Sebastian-Gambaro, F.J.Liron-Hernandez, X.Fuentes-Arderin. Intra- and Inter-Individual Biological Variability Data Bank. - Eur.J.Clin.Chem.Clin.Biochem., 1997, 35, 11, 845-852.
Для тех случаев, когда коэффициент межиндивидуальной вариации неизвестен, его условно принимают равным двум коэффициентам внутрииндивидуальной вариации:
CVG = 2 CVI (1)
Требования к целевому значению смещения формулируются в виде неравенства:
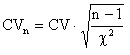 (2)
(2)
Целевое значение общего коэффициента аналитической вариации не должно превышать 0,5 коэффициента внутрииндивидуальной вариации:
CV < 0,5 CVI (3)
Значения коэффициентов внутрииндивидуальной и межиндивидуальной вариации для различных показателей, взятые за основу для расчетов, приведены в таблице 2 настоящего приложения.
2.3. Принципы расчета допустимых пределов погрешностей.
Воспроизводимость метода характеризуется коэффициентом вариации. Оценка ее проводится по результатам однократного анализа однородного материала в 10 или 20 аналитических сериях. Предельно допустимое значение коэффициента вариации в n аналитических сериях рассчитывается по следующей формуле:
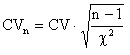 ,
(4)
,
(4)
где c2 - критерий Пирсона с уровнем значимости 0,05 и числом степеней свободы (n-1). Если n=10, c2=3,33. Если n=20, c2=10,12.
Правильность метода характеризуется величиной относительного смещения среднего от установленного значения. Оценка ее проводится по результатам однократного анализа однородного аттестованного материала в 10 или 20 аналитических сериях. Предельно допустимое значение величины относительного смещения рассчитывается по формуле:
![]() ,
(5)
,
(5)
где 1,96 - квантиль стандартного нормального распределения для уровня значимости 0,05.
Биологически обоснованные ПДЗ погрешностей клинических лабораторных исследований приведены в таблице 2.
Руководитель Департамента
организации медицинской
помощи населению А.А.Карпеев